Galvanische Korrosion und wie sie verhindert werden kann
Wann fließt elektrischer Strom?
Damit Strom fließen kann, werden zwei Elemente benötigt – wir brauchen einen Potenzialunterschied und es muss ein geschlossener Stromkreis vorliegen. Dies kennen wir von unserem Bordstromnetz, in der die Batterie für den Potenzialunterschied im jeweiligen Stromkreis sorgt.
Wann fließt galvanischer Strom?
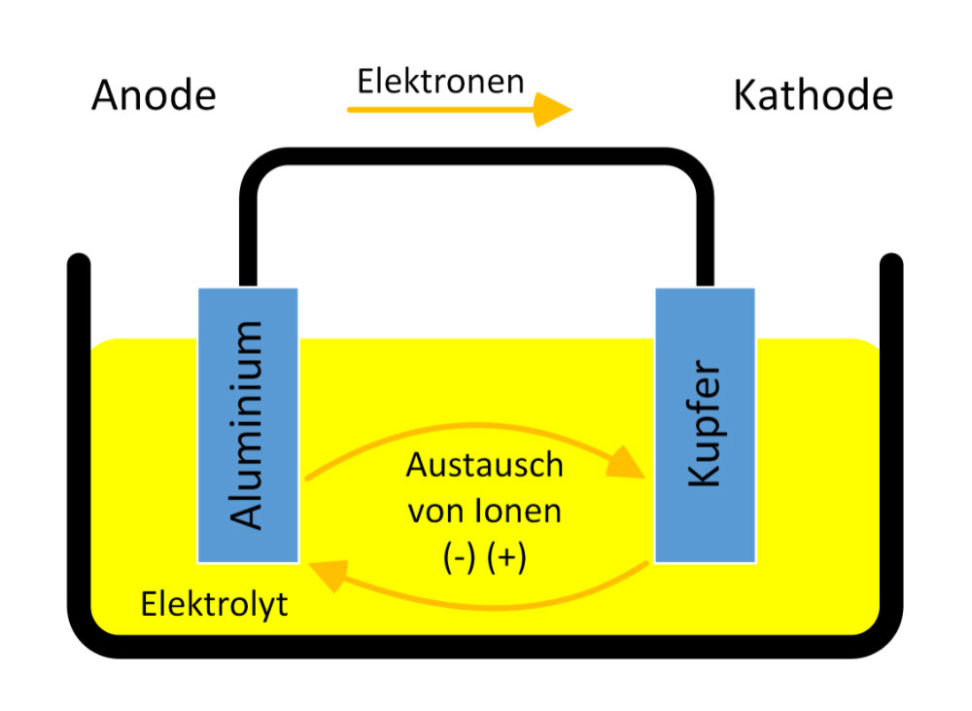
In einer galvanischen Zelle werden drei Elemente für einen Stromfluss benötigt – zwei elektrochemisch unterschiedliche Metalle mit unterschiedlichem elektrischem Potenzial, diese müssen über einen elektrischen Leiter verbunden sein und dann ein Elektrolyt über welches der Fluss der Metallionen stattfindet.
Bei dem Elektrolyten kann es sich um unterschiedliche Flüssigkeiten handeln, z.B. Regenwasser, Salzwasser oder auch Säuren und Laugen.
Das Metall mit dem höheren elektrischen Potenzial wird zur Anode und das mit dem niedrigeren zur Kathode. Der Strom fließt von der Anode zur Kathode. Die Anode löst sich auf, bzw. korrodiert und bildet Ionen. Diese werden dann an das Elektrolyt abgegeben, wo sie in der Lösung bleiben oder mit anderen Ionen wieder reagieren. Das unedlere Metall löst sich auf – hier spricht man von galvanischer Korrosion.
Übertragen auf den maritimen Bereich kennen wir alle den Effekt, dass Schrauben, Bootsrümpfe, Masten und Bäume, Saildrives oder Z-Antriebe, Propeller, etc. sich langsam auflösen, weil Ionen abgegeben werden und sich das Metall zersetzt.
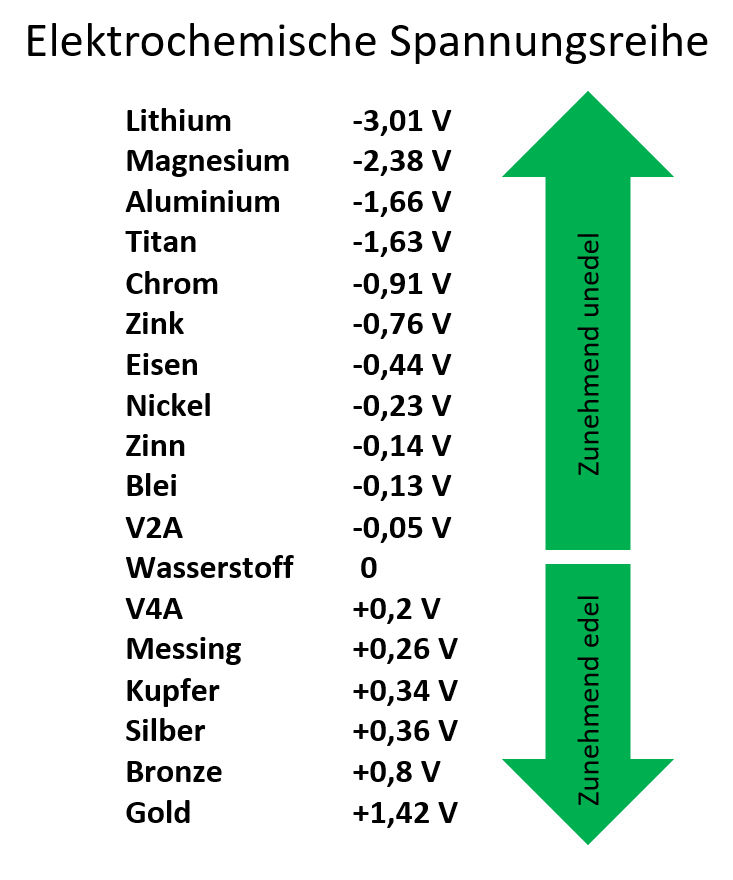
Elektrochemische Spannungsreihe
Galvanische Korrosion auf Booten / Gefahren und Lösungen
Beispiel 1

Auf einem Boot oder einer Yacht mit z.B. einem Kunststoff-Rumpf, einer Batterie, Motor und Getriebe, VA-Antriebswelle, Bronze-Propeller, VA-Ruderwelle, Alu-Ruderlager, Zinkanoden und zu guter Letzt ein kupferbasierendes Antifouling. Die Bordinstallation verfügt über einen Potenzialausgleich, die den elektrischen Leiter darstellt. Wird das Schiff jetzt ins Wasser gelegt, kommt das noch fehlende Elektrolyt ins Spiel und die galvanische Zelle ist vollständig. In diesem Beispiel haben wir gleich mehrere Zellen: den Bronze-Propeller und die VA-Welle, die Zinkanoden und den Kupferanstrich sowie das Alu-Lager der Ruderwelle. Das Problem ist, dass der Strom immer den Weg des geringsten Widerstandes geht. Ist ein Metall geopfert (Zinkanode oder Alu-Lager) geht es unter anderen Metallen weiter bis keine Potenzialunterschiede mehr vorhanden sind.
Beispiel 2 – Landstrom

Wenn wir uns mit dem Landstrom verbinden, holen wir uns in den meisten Fällen auch den Schutzleiter und damit das Landpotential an Bord. Wenn die Spundwand aus Stahl ist, ist eine weitere galvanische Zelle vorhanden, da wir über den Schutzleiter eine elektrische Verbindung erhalten. Weiter ist es durchaus möglich, dass das Landpotential des Schutzleiters aus der Landstromsäule und das der Spundwand leicht unterschiedlich sind. Auch dieser Potenzialunterschied hat dann einen Ausgleichsstrom zum Land zur Folge – zusätzlich zu den anderen möglichen Galvanikherden.
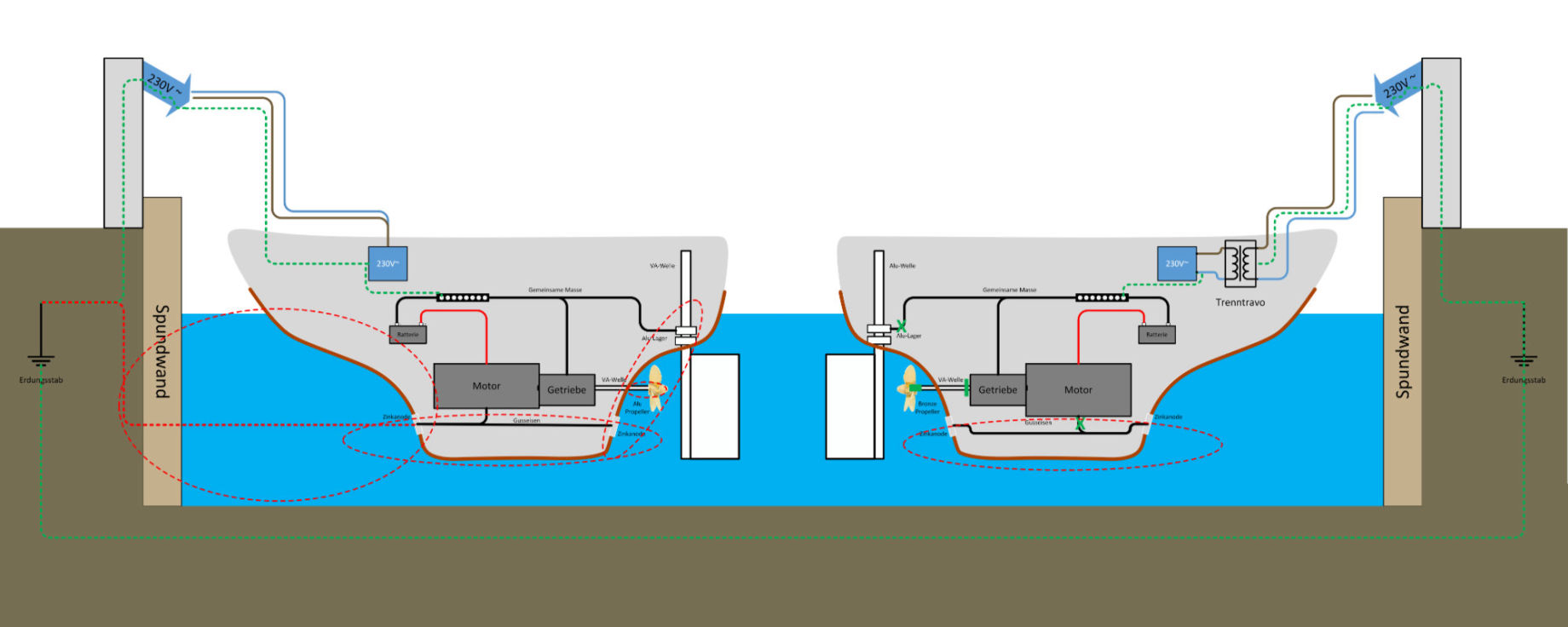
Beispiel 3 – Zwei Schiffe im Hafen
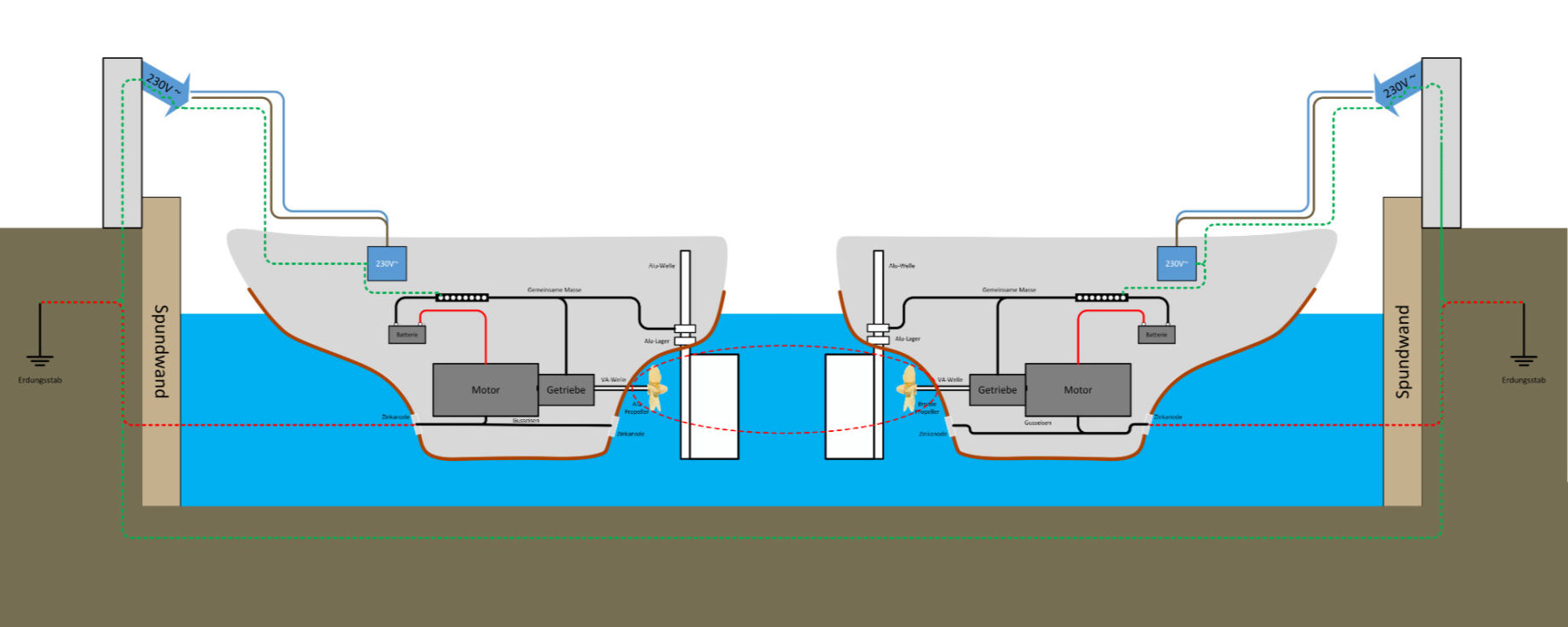
Zwei Schiffe im Hafen sind mit Landstrom verbunden und beide haben ihre bereits vorher genannten galvanischen Stromzellen an den Rümpfen. Über den Schutzleiter des Landstroms besteht jetzt eine elektrische Verbindung der beiden Schiffe. Damit sind hier alle Bedingungen für einen galvanischen Stromfluss erfüllt. Hat das eine Schiff einen Alu- und das andere einen Bronzepropeller, wird der Alu-Propeller sich langsam auflösen. Auch vor anderen Potenzialunterschieden der Elektrochemischen Spannungsreihe zwischen den Schiffen wird die Galvanik nicht haltmachen.
Was kann man dagegen tun?

Wenn wir eine der drei Voraussetzungen für eine galvanische Zelle eliminieren, kann kein galvanischer Strom fließen. Die unterschiedlichen Metalle und das Elektrolyt können wir nicht immer beeinflussen – bleibt nur die elektrisch leitende Verbindung. Heben wir diese auf, spricht man von einer galvanischen Trennung.
Wir trennen also die Ruderanlage von der gemeinsamen Masse, so auch die Zinkanoden. Wir trennen die Antriebswelle galvanisch durch Einbringen eines nicht leitenden Werkstoffes, so auch den Propeller auf der Antriebswelle. Und wir installieren einen Trenntrafo, der das Landstromnetz vom Bord-Netz galvanisch trennt.
Überall dort, wo eine galvanische Trennung unmöglich erscheint, müssen wir Opferanoden anbringen, die wiederum, um eine perfekte Wirkung zu erzielen, sehr gute leitende Verbindungen haben müssen. Außerdem müssen wir diese unbedingt beobachten. Sind sie verbraucht, oder ist ihre Oberfläche oxidiert, ist die Funktion der Opferanode eingeschränkt und es könnte doch ein anderes, nicht gewünschtes Metall zerfressen werden.
Um galvanische Ströme und galvanische Korrosion auszuschließen, muss eine konsequent galvanische Isolation von Rumpf und Bordsystem als auch von unterschiedlichen Metallen durchgeführt werden. Elektrisch leitende Verbindungen (dies kann auch feuchtes/nasses Holz bei Holzrümpfen sein) zwischen unterschiedlichen Metallen, die wiederum über einen Elektrolyten verbunden sind, sind unbedingt zu verhindern.
Nur eine einzelne Masseverbindung von einem Gerät zum Rumpf genügt, um die galvanische Isolation aufzuheben und die Galvanik wieder in Gang zu setzen. Diese Verbindung muss nicht über eine Leitung stattfinden, sie kann auch über eine Befestigungsschraube oder sich bildende Feuchtigkeit erzeugt werden.
Ob ein Bordsystem und der Rumpf sauber voneinander getrennt sind, kann über eine regelmäßige Isolationsmessung überprüft werden. Auch eine feste Isolationsmesseinheit in einem Bordsystem, die bei einer Veränderung des Isolationswiderstandes warnt, ist vor allem bei Alu-Yachten sehr zu empfehlen. Aber auch Holzrümpfe sind, was galvanische Korrosion angeht, sehr stark gefährdet und sollten stets überwacht und überprüft werden.
