Wann fließt galvanischer Strom?
In einer galvanischen Zelle
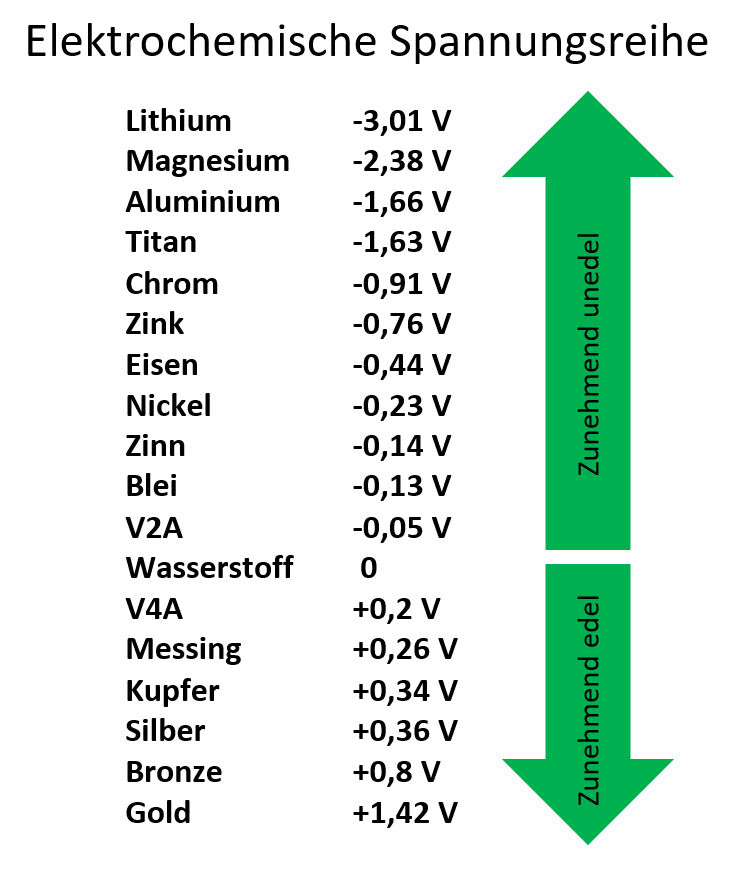
werden drei Elemente für einen Stromfluss benötigt – zwei elektrochemisch unterschiedliche Metalle
mit unterschiedlichem elektrischem Potenzial, diese müssen über einen elektrischen Leiter verbunden
sein und dann ein Elektrolyt über welches der Fluss der Metallionen stattfindet.
Bei dem Elektrolyten kann es sich um unterschiedliche Flüssigkeiten handeln, z.B. Regenwasser,
Salzwasser
oder auch Säuren und Laugen.
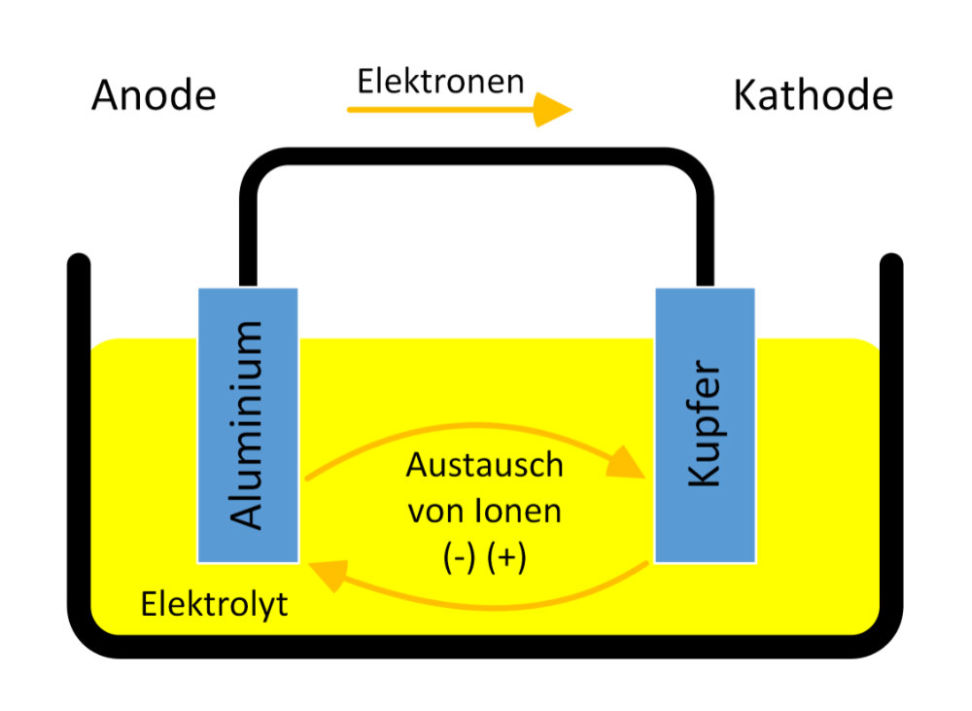
Das Metall mit dem höheren elektrischen Potenzial wird zur Anode
und das mit dem niedrigerem zur Kathode. Der Strom fließt von der Anode zur Kathode. Die Anode löst
sich auf, bzw. korrodiert und bildet Ionen. Diese werden dann an das Elektrolyt abgegeben, wo sie in
der Lösung bleiben oder mit anderen Ionen wieder reagieren. Das unedlere Metall löst sich auf, hier
spricht man von Galvanischer Korrosion.
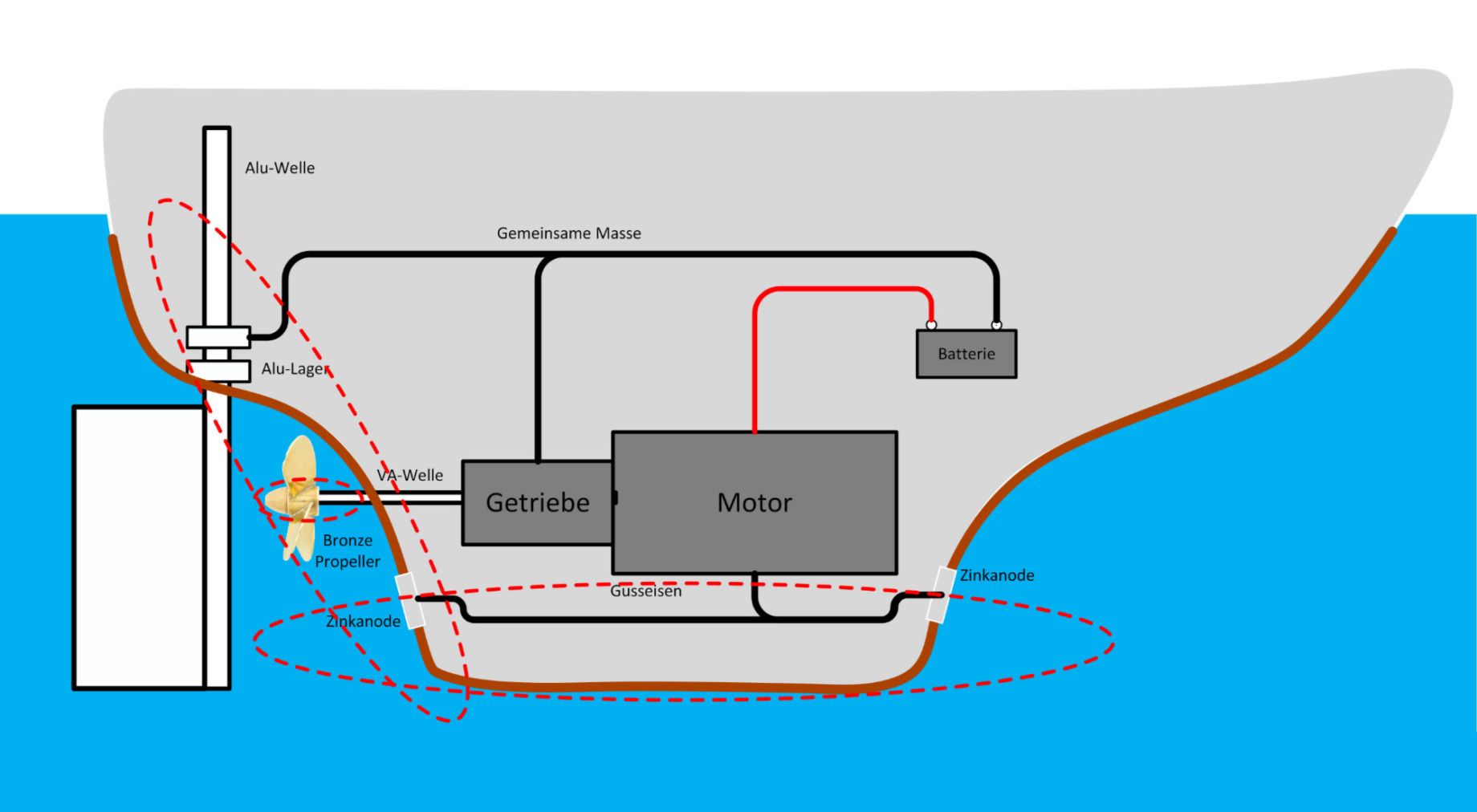
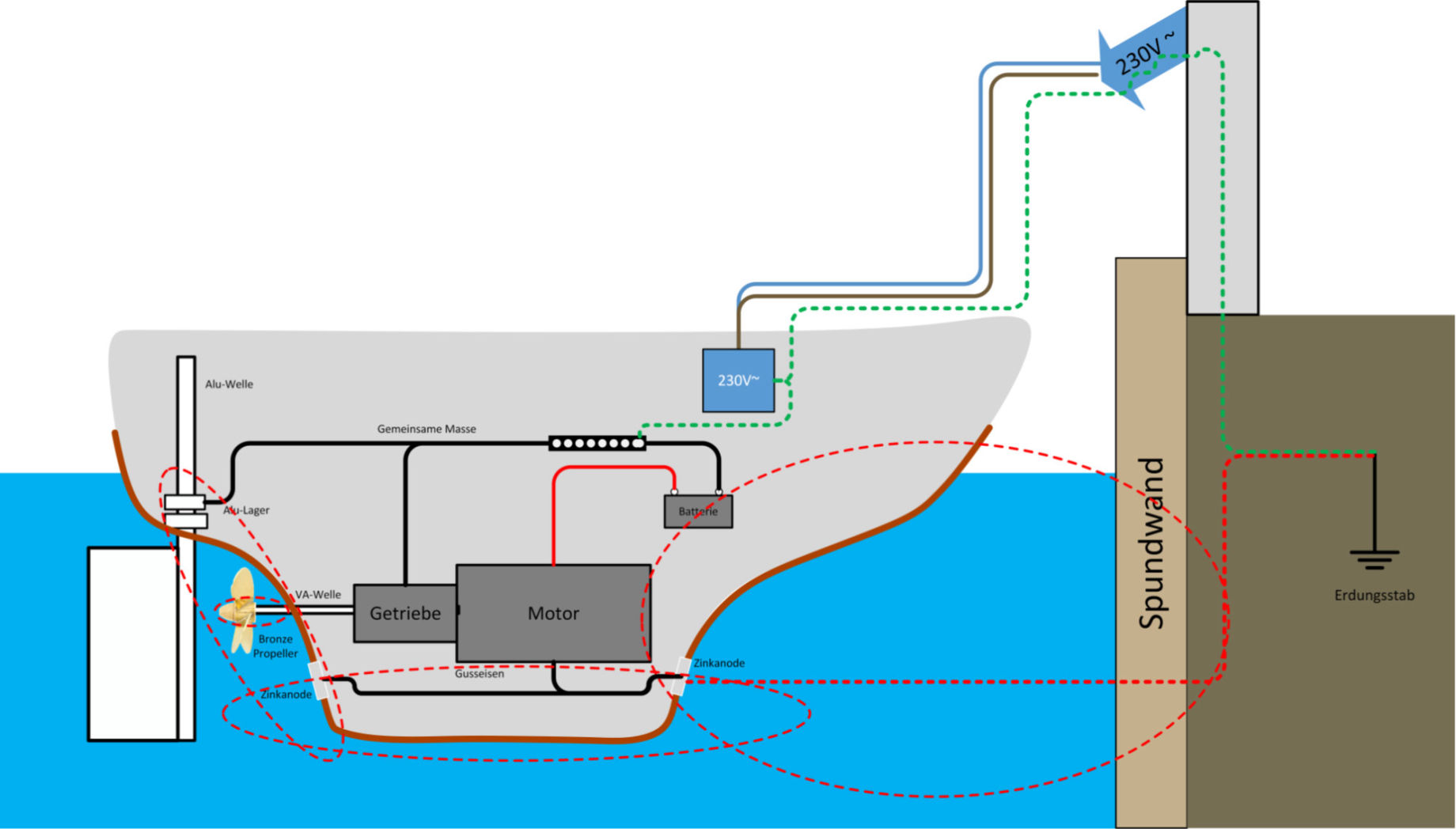
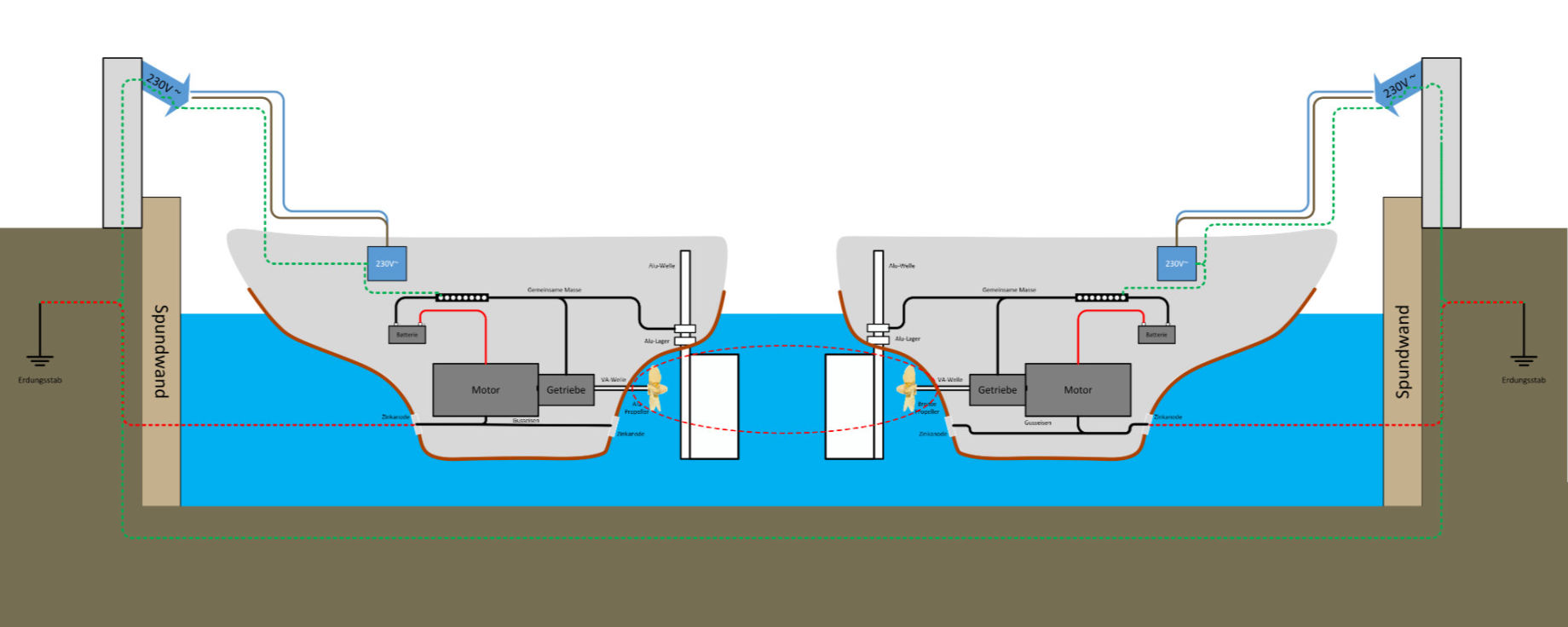
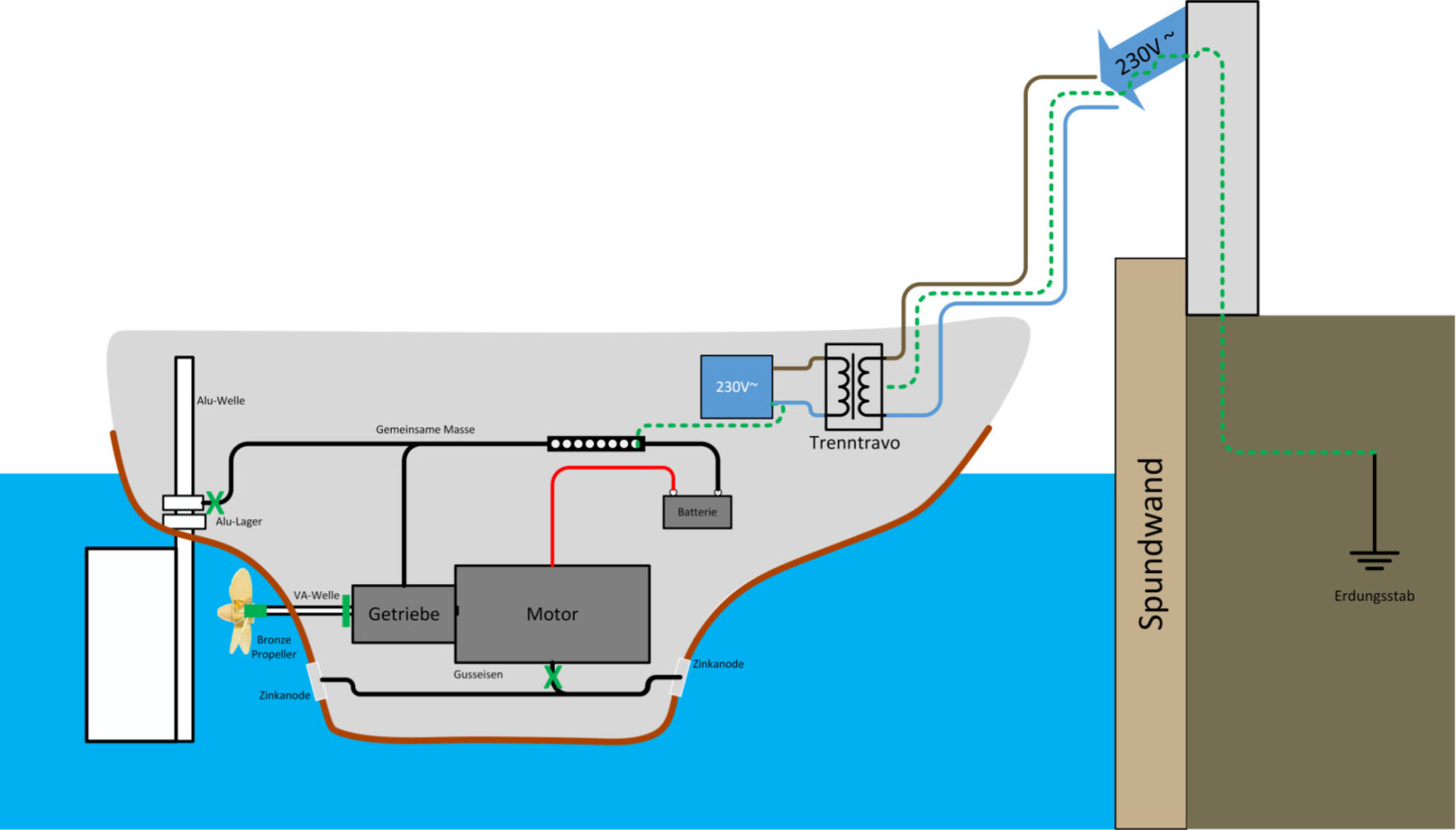
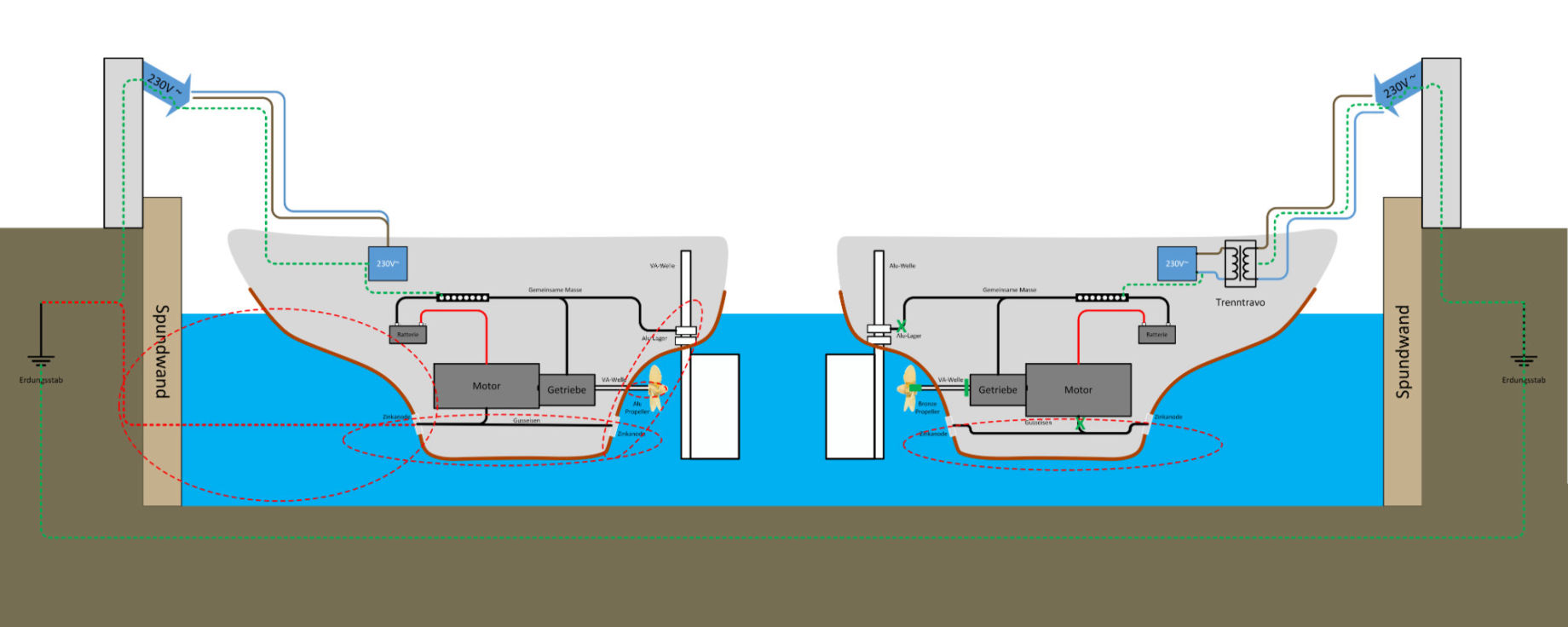
Übertragen auf den maritimen Bereich kennen wir alle
den Effekt, dass Schrauben, Bootsrümpfe, Masten und Bäume, Saildrives oder Z-Antriebe, Propeller,
etc. sich langsam auflösen, weil Ionen abgegeben werden und sich das Metall zersetzt.